

生物程序工程期末報告
Herceptin 的簡介與發展
878213 劉家齊
前言
Herceptin R (Trastuzumab)是一種治療乳癌的新藥,專門治療因過度表現人類表皮生長因子第二受體(human epidermal growth factor receptor 2, HER2)之乳癌患者。此種新藥已被美國食品藥物檢驗局(FDA)核可進入第三期臨床實驗。通常乳癌患者的治療有外科手術切除與化學療法。Herceptin是經過基因重組的方式所產生的人類化抗體,對人類表皮生長因子第二受體有非常高的親和性,因此只能特定使用在人類表皮生長因子第二受體大量表現的乳癌患者上,而這種乳癌患者約佔所有乳癌患者中25-30%的比率。在人類表皮生長因子第二受體的過度表現的乳癌患者,他們的癌症細胞上帶有大量的人類表皮生長因子第二受體,其他的細胞則含量很少,因此成為可以鑑識用的標記。此外,人類表皮生長因子第二受體的大量表現促使細胞大量複製繁殖,進而發展成癌症細胞。
Genentech公司基於人類表皮生長因子第二受體為乳癌的一種標記蛋白,並且其為引發癌症的因素之一,因此開發出Herceptin這種治療性抗體。為了避免外來抗體引起身體內的免疫反應,Herceptin是製成人類化單株抗體,此種方式也是第一種治療乳癌的抗體。在患者的治療上,必須先進行人類表皮生長因子第二受體的免疫測定,以確定是否有人類表皮生長因子第二受體大量表現,才能給予投藥。Herceptin也可與以接收化學療法的患者同時使用,或是給予無法進行化學治療的患者使用。
Herceptin藥品簡介
Herceptin R (Trastuzumab)是一種重組DNA的人類化單株抗體,最於人類表皮生長因子第二受體在細胞外的區域有很高的親和性,以細胞基質試驗(cell-based assay)測定其Kd= 5nM。這個抗體是IgG1 kappa的形式,主架構為人類抗體的部份,重組上可與人類表皮生長因子第二受體互補4D5老鼠抗體的部份,形成人類化單株抗體。
生產此人類化單株抗體的方式,是使用中國蒼鼠卵巢細胞(Chinese Hamster Ovary, CHO)進行懸浮培養的量產。在培養基內有使用抗生素gentamicin,但在最後的產品上已將此抗生素去除。
Herceptin產品是一種無菌、淡黃色、不含防腐劑的親水性粉末,以靜脈注射方式施打。每一管Herceptin包含440mg的Trastuzumab、9.9 mg L-histidine HCl、6.4 mg L-histidine、400 mg a,a-trehalose dihydrate與1.8 mg polysorbate 20。製備的方法是將20 ml的注射級無菌水加入得到21 ml的溶液,Trastuzumab約為21 mg/ml的濃度並且溶液pH為6。
人類表皮生長因子第二受體的研究
人類表皮生長因子第二受體的基因HER2 gene,先前的研究被稱為neu或c-erbB-2,是一個185-kDa的transmembrane tyrosine/kinase receptor,標記為p185HER2,與其他細胞膜上的EGFR family蛋白有部份的同源性。人類表皮生長因子第二受體是在1995年所定義的蛋白質,研究人員開始了解過度表現的人類表皮生長因子第二受體在乳癌上所辦顯得角色。人類表皮生長因子第二受體在25-30%的乳癌患者上,可以發現其過度表現的情形。研究發現抗體直接接合在p185HER2上,可以抑制過度表現p185HER2之癌細胞的增長與轉移。先前的研究從老鼠所得之抗體MAB 4D5為直接抗p185HER2區域的抗體,在實驗室內的實驗結果可以抑制人類表皮生長因子第二受體過度表現的人類乳癌細胞。
直接標的人類表皮生長因子第二受體之抗體的專利
United States Patent
Patent Number: US5677171
Hudziak; Robert M., et. al.
Date of Patent: Oct. 14, 1997
MONOCLONAL ANTIBODIES DIRECTED TO THE HER2 RECEPTOR
Inventors:
Hudziak; Robert M. (Corvallis, OR)
Shepard; H. Michael (Rancho Santa Fe, CA)
Ullrich; Axel (Portola Valley, CA)
Fendly; Brian M. (Half Moon Bay, CA)
Assignee:
Genentech, Inc. (South San Francisco, CA; Assignee type: U.S. Company or Corporation)
Appl. Number: 94US-286303
Filed: Aug. 5, 1994
Related U.S. Application data
This application is a continuation of Ser. No. 07/977,453, filed Nov. 18, 1992, now abandoned, which is a continuation of Ser. No. 07/147,461, filed Jan. 25, 1988, now abandoned, which is a continuation-in-part of Ser. No. 07/143,912, filed Jan. 12, 1988, now abandoned, which applications are incorporated herein by reference and to which applications priority is claimed under 35 U.S.C. .sctn. 120.
Int. Cl.-6
6-C07K-016-0000, 6-G01N-033-0574
U.S. Cl.
435240270, 530388800, 530388850, 530387700, 435007230, 435172200
Field of Search
530387700, 530388800, 530388850, 530381100, 435007230, 435240270, 435172200, 435070210
專利的構想
此發明物的構想,利用抗原引發免疫反應的方式,從骨髓細胞內刺激出可以抗HER2人類表皮生長因子第二受體的淋巴球細胞,並且在篩選出此種淋巴球後與持續生長的細胞株融合,成為可持續增殖並生產anti-HER2抗體之融合細胞株。生產出的抗體對人類表皮生長因子第二受體有高度的專一性,可以接合於此受體在細胞膜外的區域。在多株抗體中,只要有專一性接合人類表皮生長因子或人類表皮生長因子受體也可能被使用。
此重組抗體的功能可以用於癌症的治療上。在試管內的研究中顯示超過20%機率有抑制癌細胞增殖的效果,超過50%的癌細胞不會變大。因此,此anti-HER2抗體的附加應用,將使用在抑制因血清刺激受體導致癌症的治療。
單株抗體具有高專一性且直接接合至抗體的單一區域,多株化抗體則包含多種結合抗原不同區域的抗體,相較之下單株抗體更能直接標定抗原。單株化抗體在抗原與抗體接合的原理下,能改進診斷的篩選與免疫分析應用。此外,藉由融合瘤細胞的方式,能得到單純的單株抗體。單株抗體的獲得可能以培養融合瘤細胞回收上清液或是將融合瘤細胞打入老鼠腹腔收集腹水。融合瘤細胞技術以Kohler and Milstein, Eur. J. Immunol. 6, 511 (1976)所發表的方法得到細胞株,可以得到高濃度的單株抗體以標定許多特定的抗原。
融合瘤細胞株可以在生物體外以細胞培養基進行培養。在此發明物所使用的細胞株篩選是利用hypoxanthine-aminopterin-thymidine (HAT)medium篩選出,然後建立持續培養的細胞株。融合瘤細胞株的儲存則是以液態氮冰凍儲存,冰凍的細胞株可以隨時解凍進行培養病能持續分泌單株抗體。回收分泌出的單株抗體並去除雜質將以離心沈澱、離子交換樹酯、親和性柱狀層析..等方式進行。
整個發明物以老鼠的單株抗體作舉例,但實際並不侷限以老鼠的抗體製作,人類的抗體將可能被使用或被改良至較為時宜。利用人類融合瘤細胞株得到抗體的方式如Cote et al., Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, p. 77 (1985).,或是發展成"chimeric antibodies" (Morrison et al., Proc. Natl. Acad. Sci. 81, 6851 (1984); Neuberger et al., Nature 312, 604 (1984); Takeda et al., Nature 314, 452 (1985)) ,應用從老鼠的抗體上切出接合抗原的區域與人類的抗體組合(such as ability to activate human complement and mediate ADCC)。產生此發明物的過程,具有較大範圍的彈性可供組合使用。
抗體實際的生產方式
從老鼠中篩選出對HER2有高親和性的單株抗體MAb 4D5,經實驗測試後此抗體對過度表現人類表皮生長因子第二受體的癌症細胞。由於老鼠的抗體施打於人類上將引起免疫反應,減低其使用的效果。因此將此MAb 4D5進行人類化抗體的改造,保留MAb 4D5的抗原接合區與人類的IgG kappa 組合,完成人類化抗體rhuMab HER2 (Trastuzumab)。
人類化抗體rhuMab HER2的基因轉殖進入至中國蒼鼠細胞(CHO)內,可以持續生產此抗體。細胞培養於細胞用培養基內,並添加抗生素gentamicin進行抗體的生產。回收上清液後,雜質經以離心沈澱、離子交換樹酯與親和性柱狀層析等過程,得到精製的rhuMab HER2抗體,抗生素gentamicin亦被除去未殘留於最後的產物中。
人類表皮生長因子第二受體過度表現的偵測
由於rhuMab HER2抗體是要用於人類表皮生長因子第二受體有過度表現的乳癌患者,因此需要先鑑定乳癌患者是否為受體過度表現,才能以抗體進行治療。美國食品藥物檢驗局已同意以DAKO HercepTest assay來偵測是否為人類表皮生長因子第二受體過度表現的患者。
動物實驗
Recombinant Humanized Anti-HER2 Antibody (HerceptinTM) Enhances the Antitumor Activity of Palitaxel and Doxorubicin against HER2/neu Overexpressing Human Breast Cancer Xenografts
Jose Baselga, Larry Norton, Joan Albanell, Young-Mee Kim, and John Medelsohn
Cancer Research 58:2825-2831 (1998).
在進行臨床實驗前必須先要建立動物模式,以了解新藥是否有其效果。此篇作者自Genentech公司取得rhuMab HER2抗體,在癌細胞與移植腫瘤的老鼠身上試驗其效果,並且與其他用於化學治療的藥物同時施用,以比較rhuMab HER2抗體在動物體內的療效。
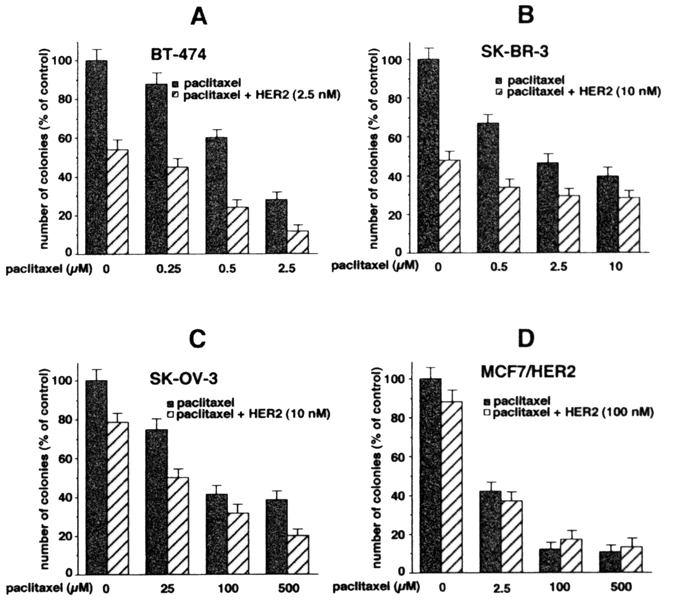
結果一:BT-474、SK-BR-3與SK-OV-3三株細胞株均為HER2過度表現之細胞,MCF7/HER2細胞則無HER2表現。在前三株細胞中,paclitaxel+HER2比只添加paclitaxel在抑制癌細胞上效果較好,然而在MCF7/HER2細胞則無明顯差異。
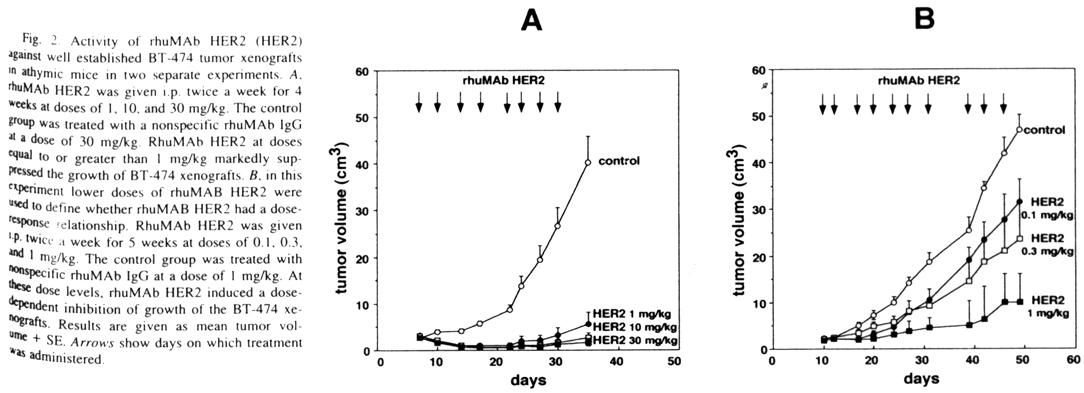
結果二:不同濃度的rhuMab HER2抗體加至BT-474細胞內,以1 mg/kg以上的濃度均有明顯的抑制效果(圖A);將濃度再向下稀釋,則越低的濃度越無法抑制癌細胞的增長。
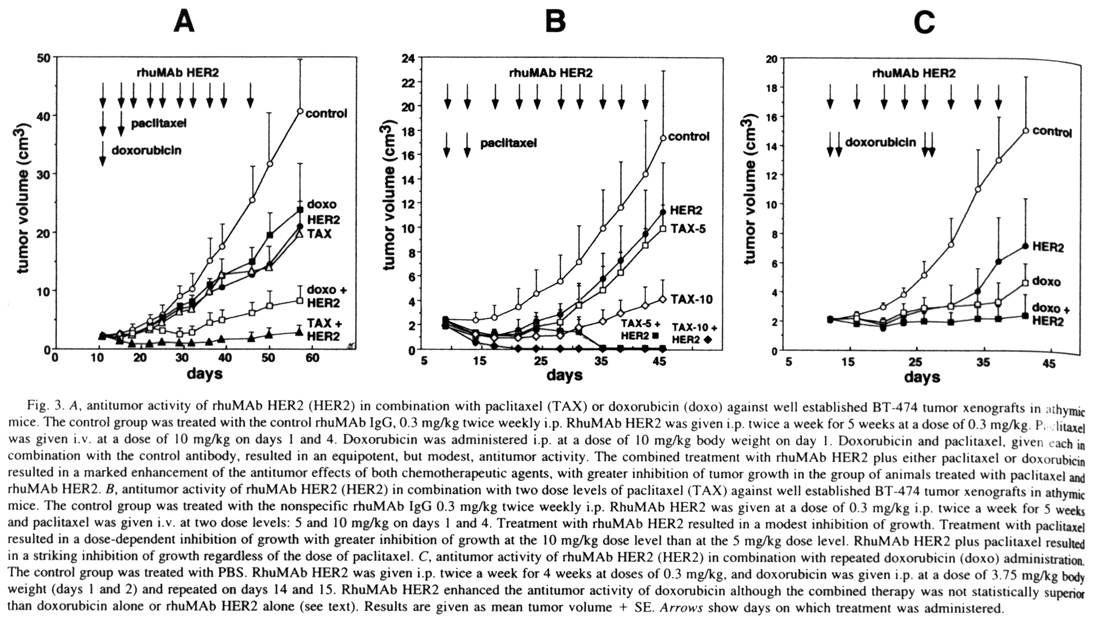
結果三:rhuMab HER2抗體與其他藥物(doxo, TAX-5)同時施用,比起每個藥物單獨使用能更有效地抑制癌細胞。

實驗結果總結:rhuMab HER2抗體能抑制癌細胞,提高老鼠的存活率。再與其他藥物配合之下,更能有效地抑制癌細胞的增殖提高個體的存活。
人體臨床實驗
三個第一期臨床實驗與二個第二期臨床實驗的結果已經完成。患者注射的劑量在第一次使用4 mg/kg,而後每個星期注射2 mg/kg。
單獨使用rhuMab HER2抗體的患者共有222名,其中有16%的患者的病情好轉,4%病人則完全治癒,12%病人有腫瘤縮小的狀況。試驗時期在6周到18個月,藥物的半使用時間為9個月。
rhuMab HER2抗體與其他藥物共同使用的患者共有469名,共同使用的藥物為paclitaxel或是doxorubicin + cyclophosphamide (DC)這二組。超過25%的患者其癌細胞停止生長,而後隨施用時間的增加而提高至65%。32-48%的患者其癌細胞逐漸萎縮並減輕病徵。其中以paclitaxel共同使用的效果較佳,有42%的患者呈陽性反應,單獨使用paclitaxel只有16%患者呈陽性反應。rhuMab HER2 + DC只有比DC高9%的患者呈陽性反應。藥物的半使用時間為7.2個月。一年後的存活率為79%,比化學療法68%高。
過敏測試
903名受試者經由human anti-human antibody (HAHA)的測定下,只有一人被測出有trastuzumab,並無任何人有過敏的症狀。
致癌因子測定
沒有任何檢驗證實trastuzumab有致癌的趨勢。
突變因子測定
以5000 g/ml的trastuzumab用Ames tests作六種測試用細菌的測定,結果沒有任何證據顯示會造成基因突變。以人類淋巴球添加5000 g/plate的trastuzumab並沒有發現有細胞異常的變化。在活體的突變測試(micronucleus assay),使用118 mg/kg的trastuzumab並沒有證據顯示對老鼠的骨髓細胞(bone marrow cell)造成染色體異常。
對孕婦的傷害
以懷孕的母猴每週施以2 mg/kg trastuzumab,在連續25周後並沒有發現對胎兒有所傷害。
保存期限與儲存
每管的Herceptin在配製前可以一直穩定地保存在2-8℃,以注射級無菌水配製後在2-8℃下只能維持28天,超過以上的期限則必須丟棄,且不能冰凍於0℃以下。配製後在室溫下只能維持24小時,因此施打後的剩餘溶液或超過24小時的期限,則必須丟棄不能再使用。
副作用
在40%的受試者第一次施打Herceptin後,有輕微發熱與頭疼的現象。在與化學治療同時共用的情況下,有部份受試者有掉頭髮、嘴角潰爛與血球數偏低的現象,但在單獨使用Herceptin則無這些現象。
在心臟病患者使用Herceptin後,有官能不良的情形出現。因此對於心臟病患者尚以保留的態度不建議使用Herceptin,還須等待進一步的研究。
總結
一個治療性的新藥的發展,從構想開始至臨床試驗是需要經過長時間的研究。這是第一個利用單株抗體治療乳癌的方法,從前面的資料我們可以了解一個新藥需要專利的保護,要有動物模式的建立後,才能進入臨場試驗。藥物的生產過程要以安全方式量產,並且新藥也要進行可能的副作用及突變測試,方能說服國家檢驗單位的上市許可。HER2 gene自1995年定義後,做成藥物的構想在1997年獲得專利,1998年FDA允許Herceptin做臨床試驗,至今年1999年已被允許進入第三期臨床試驗。對於發展一個治療性的新藥,提供我們很好的示範例子。
生產公司
Genentech Inc.