B型肝炎病毒簡介
一、肝炎病毒
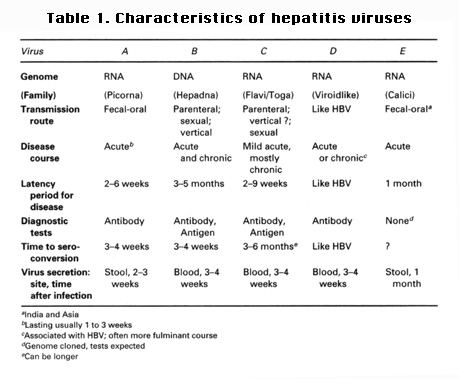
肝炎病毒分為A、B、C、D、E五種,其中除了B型肝炎是DNA病毒
外,其他四種皆為RNA病毒。五種肝炎病毒的比較,如傳染途徑、潛伏
期、診斷方法等等,皆詳細列於表一。其中以B型肝炎病毒為生物醫學
界研究的重點,因為其不只引起肝炎,還與肝癌的形成關係密切,甚至
是提供外殼給D型肝炎病毒,成為HDV的輔助病毒。以下是針對B型肝炎
病毒所蒐集到的資料:
 二、B型肝炎病毒
Hepatitis B Virus(HBV),過去稱為serum hepatitis virus,是在60
年代晚期找到的感染源,透過血液或體液傳染;致死率高達50%,而慢
性的B型肝炎通常會導致肝硬化及肝炎的併發。由於其以DNA為主要遺
傳物質,並與反轉錄病毒一樣使用RNA-dependent DNA polymerase來
進行基因的複製工作,故與其他相似的動物病毒(如GSHV、DHBV、
WHV等),併入一個新的科(Family),稱為HEPADAVIRIDAE。
B型肝炎病毒有幾個重要特徵:1) 由於其在人類及靈長類動物中,
肝細胞為唯一感染對象,故其在感染寄主後會快速趨向肝細胞。2) 會在
血液中產生很多無感染性的病毒抗原,例如HBsAg (B型肝炎表面抗原)
,此為診斷是否被感染的一種方法。3) 病毒會持續存在肝臟及血液中一
段滿長時間,而使病患成為B型肝炎的帶原者。以下則分別就病毒的結
構,生命週期,表面抗原等部分,詳細敘述:
(一) B型肝炎病毒的基因
二、B型肝炎病毒
Hepatitis B Virus(HBV),過去稱為serum hepatitis virus,是在60
年代晚期找到的感染源,透過血液或體液傳染;致死率高達50%,而慢
性的B型肝炎通常會導致肝硬化及肝炎的併發。由於其以DNA為主要遺
傳物質,並與反轉錄病毒一樣使用RNA-dependent DNA polymerase來
進行基因的複製工作,故與其他相似的動物病毒(如GSHV、DHBV、
WHV等),併入一個新的科(Family),稱為HEPADAVIRIDAE。
B型肝炎病毒有幾個重要特徵:1) 由於其在人類及靈長類動物中,
肝細胞為唯一感染對象,故其在感染寄主後會快速趨向肝細胞。2) 會在
血液中產生很多無感染性的病毒抗原,例如HBsAg (B型肝炎表面抗原)
,此為診斷是否被感染的一種方法。3) 病毒會持續存在肝臟及血液中一
段滿長時間,而使病患成為B型肝炎的帶原者。以下則分別就病毒的結
構,生命週期,表面抗原等部分,詳細敘述:
(一) B型肝炎病毒的基因
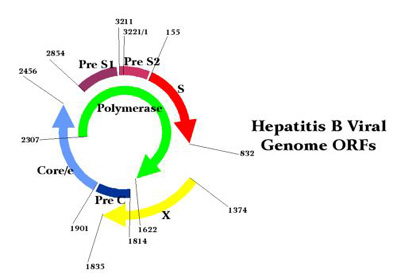 以卡通圖標示如上圖。基因的大小會因病毒副型的不同而稍有改變,
但大都在3.2 kb的長度。其特色是非完整的雙螺旋型DNA,而是有一條較
長的〝-〞型單股DNA,藉由5′端和較短的〝+〞型單股DNA形成鍵結
。病毒在寄主細胞內複製的過程,會利用反轉錄酵素,將完整長度的〝+〞
型RNA,轉錄成病毒所需的DNA基因型。參考圖二及病毒的生長週期。
病毒基因可分為三個主要的部分:1) S基因 - 主要包含病毒醣化的外
殼蛋白(glycosylated envelope protein)及核心蛋白(core protein)。
2) P基因 - 則可解碼為一個有DNA聚合酵素和反轉錄酵素活性的蛋白質。
3) X基因(或稱E) - 則是與病毒進入寄主細胞後能活化的性質有關。
以卡通圖標示如上圖。基因的大小會因病毒副型的不同而稍有改變,
但大都在3.2 kb的長度。其特色是非完整的雙螺旋型DNA,而是有一條較
長的〝-〞型單股DNA,藉由5′端和較短的〝+〞型單股DNA形成鍵結
。病毒在寄主細胞內複製的過程,會利用反轉錄酵素,將完整長度的〝+〞
型RNA,轉錄成病毒所需的DNA基因型。參考圖二及病毒的生長週期。
病毒基因可分為三個主要的部分:1) S基因 - 主要包含病毒醣化的外
殼蛋白(glycosylated envelope protein)及核心蛋白(core protein)。
2) P基因 - 則可解碼為一個有DNA聚合酵素和反轉錄酵素活性的蛋白質。
3) X基因(或稱E) - 則是與病毒進入寄主細胞後能活化的性質有關。
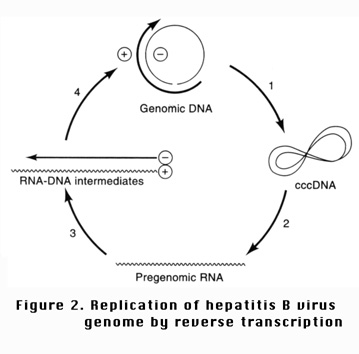 (二) B型肝炎的生命週期
(二) B型肝炎的生命週期
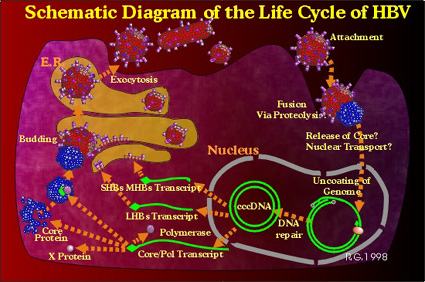 病毒要進入細胞,首先必須具專一性地連接上寄主細胞,(已知病毒
中型與大型的表面蛋白,可能與能接上肝細胞的專一性有關)。之後,病
毒的表面會與寄主的細胞膜融合,而使病毒的中心蛋白質,包括基因及聚
合酵素都能進入細胞。進入細胞後,病毒的基因在寄主的細胞核中,進行
修補及環化的工作。
完整環化的病毒DNA基因,會保存在寄主細胞核,並且同時進行三種
轉錄的工作。第一種是只轉錄中型及小型的表面抗原(middle and small
surface antigens);第二種則是轉錄大型的表面抗原;最後一種不但轉
錄整個病毒基因,還繼續轉譯RNA,表達病毒的核心、E、及聚合酵素等蛋
白質,同時也會使用反轉錄酵素製造〝-〞型DNA。另一條〝+〞型DNA
通常在成熟的病毒粒子包裝好,才會完成,至於為何如此設計的原因則還
不清楚,很可能是為了保證釋放出寄主細胞的病毒粒子,都有可進行複製
作用的DNA。
在上圖中,完整的病毒核心粒子是如出芽般進出內質網;但這只是最
有可能的說法,並不一定真的如此。成熟的病毒被釋放出寄主後,會回到
血液循環中,再尋找下一個寄主細胞。
(三)B型肝炎表面抗原
如前面所提,B型肝炎表面抗原分為small,middle及large三種;在
病毒的表面抗原基因中,由三個不同的起始點及相同的終點來進行轉錄。
不但共同使用S基因,且互相相關。以下為三個表面抗原的詳細介紹:
病毒要進入細胞,首先必須具專一性地連接上寄主細胞,(已知病毒
中型與大型的表面蛋白,可能與能接上肝細胞的專一性有關)。之後,病
毒的表面會與寄主的細胞膜融合,而使病毒的中心蛋白質,包括基因及聚
合酵素都能進入細胞。進入細胞後,病毒的基因在寄主的細胞核中,進行
修補及環化的工作。
完整環化的病毒DNA基因,會保存在寄主細胞核,並且同時進行三種
轉錄的工作。第一種是只轉錄中型及小型的表面抗原(middle and small
surface antigens);第二種則是轉錄大型的表面抗原;最後一種不但轉
錄整個病毒基因,還繼續轉譯RNA,表達病毒的核心、E、及聚合酵素等蛋
白質,同時也會使用反轉錄酵素製造〝-〞型DNA。另一條〝+〞型DNA
通常在成熟的病毒粒子包裝好,才會完成,至於為何如此設計的原因則還
不清楚,很可能是為了保證釋放出寄主細胞的病毒粒子,都有可進行複製
作用的DNA。
在上圖中,完整的病毒核心粒子是如出芽般進出內質網;但這只是最
有可能的說法,並不一定真的如此。成熟的病毒被釋放出寄主後,會回到
血液循環中,再尋找下一個寄主細胞。
(三)B型肝炎表面抗原
如前面所提,B型肝炎表面抗原分為small,middle及large三種;在
病毒的表面抗原基因中,由三個不同的起始點及相同的終點來進行轉錄。
不但共同使用S基因,且互相相關。以下為三個表面抗原的詳細介紹:
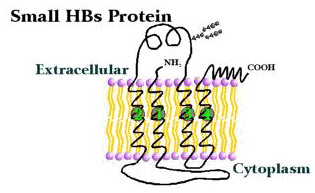
- 小型B型肝炎表面抗原(HBsAg or SHBsAg)
此蛋白質是最小的表面抗原,包含全部的S基因,也被稱為Australia
antigen。如下圖所示,其為高度的疏水性,包含了四次穿過細胞膜的部
分。它也包含了高度的抗原epitope,可利用分析這些epitope,來決定帶
原者的類型。
被病毒感染的細胞在早期會大量製造這種抗原,在帶原者的體內產
生的無致病性的HBsAg濃度,可高達200ug/ml。這些抗體的表達,與內
質網因大量的大型表面抗原的產生而受到的壓力有關。
研究免疫系統發現,若來源為T細胞的HBsAg會抑制其他T細胞產生
對抗該抗原的抗體。亦發現這種針對HBV的幾個部分,產生抗體被抑制
的現象,常見於慢性HBV的帶原者。
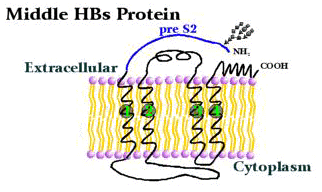
- 中型B型肝炎表面抗原(MHBsAg)
MHBsAg除了S基因外,另外包含55個胺基酸的部分,稱為Pre-S2。
結構如下圖。Pre-S2的部份為親水性,裸露在細胞膜外,且多出一個可
醣化的地方。有人提出此抗原與HBV和肝細胞的連接,及進入肝細胞有
很大關係。但另有證據顯示這並不是MHBsAg最主要的功用。
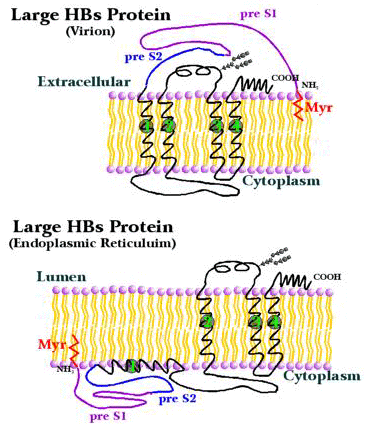
- 大型B型肝炎表面抗原(LHBsAg)
其為表面抗原中最大的,不但包括Pre-S2及S基因,還包括Pre-S1
部分。後者的序列在不同病患身上的變異很大,顯示其應為HBV和肝細
胞連結最主要的蛋白質。
如下圖所預測,此蛋白質有兩種不同的結構,分別存在於一般的成
熟病毒及內質網的表面。發現當其在內質網時,Pre-S1及Pre-S2兩部分
皆保持在細胞質內。至於其如何會穿越細胞膜到達病毒表面的原因,仍
然不清楚;有可能是透過病毒外鞘的一種特殊親水環境的小洞。
值得注意的,是雖然其為最有可能中介病毒連接到其寄主細胞的蛋
白質;但HBV真正的receptor還未被找到。
 二、B型肝炎病毒
Hepatitis B Virus(HBV),過去稱為serum hepatitis virus,是在60
年代晚期找到的感染源,透過血液或體液傳染;致死率高達50%,而慢
性的B型肝炎通常會導致肝硬化及肝炎的併發。由於其以DNA為主要遺
傳物質,並與反轉錄病毒一樣使用RNA-dependent DNA polymerase來
進行基因的複製工作,故與其他相似的動物病毒(如GSHV、DHBV、
WHV等),併入一個新的科(Family),稱為HEPADAVIRIDAE。
B型肝炎病毒有幾個重要特徵:1) 由於其在人類及靈長類動物中,
肝細胞為唯一感染對象,故其在感染寄主後會快速趨向肝細胞。2) 會在
血液中產生很多無感染性的病毒抗原,例如HBsAg (B型肝炎表面抗原)
,此為診斷是否被感染的一種方法。3) 病毒會持續存在肝臟及血液中一
段滿長時間,而使病患成為B型肝炎的帶原者。以下則分別就病毒的結
構,生命週期,表面抗原等部分,詳細敘述:
(一) B型肝炎病毒的基因
二、B型肝炎病毒
Hepatitis B Virus(HBV),過去稱為serum hepatitis virus,是在60
年代晚期找到的感染源,透過血液或體液傳染;致死率高達50%,而慢
性的B型肝炎通常會導致肝硬化及肝炎的併發。由於其以DNA為主要遺
傳物質,並與反轉錄病毒一樣使用RNA-dependent DNA polymerase來
進行基因的複製工作,故與其他相似的動物病毒(如GSHV、DHBV、
WHV等),併入一個新的科(Family),稱為HEPADAVIRIDAE。
B型肝炎病毒有幾個重要特徵:1) 由於其在人類及靈長類動物中,
肝細胞為唯一感染對象,故其在感染寄主後會快速趨向肝細胞。2) 會在
血液中產生很多無感染性的病毒抗原,例如HBsAg (B型肝炎表面抗原)
,此為診斷是否被感染的一種方法。3) 病毒會持續存在肝臟及血液中一
段滿長時間,而使病患成為B型肝炎的帶原者。以下則分別就病毒的結
構,生命週期,表面抗原等部分,詳細敘述:
(一) B型肝炎病毒的基因
 以卡通圖標示如上圖。基因的大小會因病毒副型的不同而稍有改變,
但大都在3.2 kb的長度。其特色是非完整的雙螺旋型DNA,而是有一條較
長的〝-〞型單股DNA,藉由5′端和較短的〝+〞型單股DNA形成鍵結
。病毒在寄主細胞內複製的過程,會利用反轉錄酵素,將完整長度的〝+〞
型RNA,轉錄成病毒所需的DNA基因型。參考圖二及病毒的生長週期。
病毒基因可分為三個主要的部分:1) S基因 - 主要包含病毒醣化的外
殼蛋白(glycosylated envelope protein)及核心蛋白(core protein)。
2) P基因 - 則可解碼為一個有DNA聚合酵素和反轉錄酵素活性的蛋白質。
3) X基因(或稱E) - 則是與病毒進入寄主細胞後能活化的性質有關。
以卡通圖標示如上圖。基因的大小會因病毒副型的不同而稍有改變,
但大都在3.2 kb的長度。其特色是非完整的雙螺旋型DNA,而是有一條較
長的〝-〞型單股DNA,藉由5′端和較短的〝+〞型單股DNA形成鍵結
。病毒在寄主細胞內複製的過程,會利用反轉錄酵素,將完整長度的〝+〞
型RNA,轉錄成病毒所需的DNA基因型。參考圖二及病毒的生長週期。
病毒基因可分為三個主要的部分:1) S基因 - 主要包含病毒醣化的外
殼蛋白(glycosylated envelope protein)及核心蛋白(core protein)。
2) P基因 - 則可解碼為一個有DNA聚合酵素和反轉錄酵素活性的蛋白質。
3) X基因(或稱E) - 則是與病毒進入寄主細胞後能活化的性質有關。
 (二) B型肝炎的生命週期
(二) B型肝炎的生命週期
 病毒要進入細胞,首先必須具專一性地連接上寄主細胞,(已知病毒
中型與大型的表面蛋白,可能與能接上肝細胞的專一性有關)。之後,病
毒的表面會與寄主的細胞膜融合,而使病毒的中心蛋白質,包括基因及聚
合酵素都能進入細胞。進入細胞後,病毒的基因在寄主的細胞核中,進行
修補及環化的工作。
完整環化的病毒DNA基因,會保存在寄主細胞核,並且同時進行三種
轉錄的工作。第一種是只轉錄中型及小型的表面抗原(middle and small
surface antigens);第二種則是轉錄大型的表面抗原;最後一種不但轉
錄整個病毒基因,還繼續轉譯RNA,表達病毒的核心、E、及聚合酵素等蛋
白質,同時也會使用反轉錄酵素製造〝-〞型DNA。另一條〝+〞型DNA
通常在成熟的病毒粒子包裝好,才會完成,至於為何如此設計的原因則還
不清楚,很可能是為了保證釋放出寄主細胞的病毒粒子,都有可進行複製
作用的DNA。
在上圖中,完整的病毒核心粒子是如出芽般進出內質網;但這只是最
有可能的說法,並不一定真的如此。成熟的病毒被釋放出寄主後,會回到
血液循環中,再尋找下一個寄主細胞。
(三)B型肝炎表面抗原
如前面所提,B型肝炎表面抗原分為small,middle及large三種;在
病毒的表面抗原基因中,由三個不同的起始點及相同的終點來進行轉錄。
不但共同使用S基因,且互相相關。以下為三個表面抗原的詳細介紹:
病毒要進入細胞,首先必須具專一性地連接上寄主細胞,(已知病毒
中型與大型的表面蛋白,可能與能接上肝細胞的專一性有關)。之後,病
毒的表面會與寄主的細胞膜融合,而使病毒的中心蛋白質,包括基因及聚
合酵素都能進入細胞。進入細胞後,病毒的基因在寄主的細胞核中,進行
修補及環化的工作。
完整環化的病毒DNA基因,會保存在寄主細胞核,並且同時進行三種
轉錄的工作。第一種是只轉錄中型及小型的表面抗原(middle and small
surface antigens);第二種則是轉錄大型的表面抗原;最後一種不但轉
錄整個病毒基因,還繼續轉譯RNA,表達病毒的核心、E、及聚合酵素等蛋
白質,同時也會使用反轉錄酵素製造〝-〞型DNA。另一條〝+〞型DNA
通常在成熟的病毒粒子包裝好,才會完成,至於為何如此設計的原因則還
不清楚,很可能是為了保證釋放出寄主細胞的病毒粒子,都有可進行複製
作用的DNA。
在上圖中,完整的病毒核心粒子是如出芽般進出內質網;但這只是最
有可能的說法,並不一定真的如此。成熟的病毒被釋放出寄主後,會回到
血液循環中,再尋找下一個寄主細胞。
(三)B型肝炎表面抗原
如前面所提,B型肝炎表面抗原分為small,middle及large三種;在
病毒的表面抗原基因中,由三個不同的起始點及相同的終點來進行轉錄。
不但共同使用S基因,且互相相關。以下為三個表面抗原的詳細介紹:


